Les médicaments
Le médicament n’est distribué que dans les officines de pharmacies et les pharmacies mutualistes autorisées par le gouvernement de la Nouvelle-Calédonie par arrêté. Seuls les pharmaciens et, sous leur contrôle, les préparateurs en pharmacie, ont le droit de délivrer des médicaments. Sous certaines conditions, ils peuvent également être délivrés par les dispensaires.
Les prix des médicaments sont fixés par l'application de coefficients multiplicateurs sur le prix de vente métropolitain HT.
Les prix sont majorés de 5 % dans les provinces Nord et Sud hors zone régulée, et de 7% dans la province des îles Loyauté.
Les différents types de médicaments
Définition
La définition du médicament est précisée dans l'ancien code de la santé publique (CSP) dans sa version applicable en Nouvelle-Calédonie : « On entend par médicament toute substance ou composition présentée comme possédant des propriétés curatives ou préventives à l’égard des maladies humaines ou animales [...] ». Cette définition se complète par toute substance ou composition pouvant être utilisée chez l'homme ou chez l'animal ou pouvant leur être administrée, en vue d'établir un diagnostic médical ou de restaurer, corriger ou modifier leurs fonctions physiologiques en exerçant une action pharmacologique, immunologique ou métabolique.
Les préparations magistrales réalisées à l’officine ou à l’hôpital, les contraceptifs hormonaux, les produits présentés comme supprimant l'envie de fumer ou réduisant l'accoutumance au tabac, notamment, sont des médicaments.
Le médicament homéopathique
Le médicament homéopathique est défini comme tout médicament obtenu à partir de substances appelées souches homéopathiques, selon un procédé de fabrication homéopathique décrit par la pharmacopée. Les substances ou souches de base de l’homéopathie ont trois origines : végétales, animales et minérales ou chimiques.
Le médicament à base de plante(s)
Le médicament à base de plante(s) est défini comme tout médicament dont les substances actives sont exclusivement une ou plusieurs substances végétales ou préparations à base de plantes ou une association de plusieurs substances végétales ou préparations à base de plantes. Tout comme les médicaments produits par l’industrie pharmaceutique, les plantes médicinales contiennent des substances actives pouvant être dangereuses. Les médicaments à base de plantes doivent, comme n'importe quel autre médicament, faire l'objet d'une autorisation de mise sur le marché et donc d'une évaluation du rapport bénéfice-risque.
Quelle différence entre médicament générique et princeps ?
Lorsqu’un laboratoire pharmaceutique développe et produit un nouveau médicament, celui-ci est breveté pendant une période déterminé. Cela veut dire qu’il est le seul autorisé à produire et commercialiser le médicament (ceci afin de pouvoir amortir les investissements de recherches qu’il a dû entreprendre et lui assurer des bénéfices qui pourront, en partie, être réinvestis dans la recherche de nouveaux médicaments). C’est le médicament appelé « princeps ». Il s'agit en quelques sortes du médicament « original ».
Une fois la durée du brevet arrivée à terme, d’autres laboratoires pharmaceutiques peuvent, à leur tour, produire et commercialiser le médicament : ce sont les médicaments « génériques ».
Les médicaments génériques sont donc une classe de médicaments contenant les mêmes principes actifs, en même quantité qu'un médicament princeps.
Les médicaments génériques sont vendus le plus souvent sous le nom de leur dénomination commune internationale. Leurs propriétés sont identiques à celles du princeps, de même que leur présentation, leur mode d'emploi et leur biodisponibilité au sein de l'organisme. Pour qu'un médicament générique puisse être mis sur le marché, il doit obtenir une autorisation de mise sur le marché délivrée par les autorités de santé. Ainsi, les médicaments génériques répondent aux mêmes critères de qualité et de sécurité que les princeps.
La différence entre les médicaments génériques et les princeps est principalement économique : les princeps coûtent plus cher car, pour les mettre au point, des recherches, des études et des essais cliniques extrêmement onéreux ont dû être mis en place. Les médicaments génériques, coûtent moins cher car ils ne nécessitent pas toutes ces années de recherche très couteuses puisqu’ils sont, en quelque sorte, une « copie » du princeps.
L'autre différence concerne les excipients. En effet, les médicaments génériques contiennent les mêmes principes actifs que les médicaments princeps, mais les excipients peuvent être différents. Un excipient est une substance autre que la substance active, destinée à apporter une consistance, un goût, une couleur, une stabilité à un médicament. Tout en évitant toute interaction avec le principe actif, les excipients permettent également d'amener le principe actif à l'endroit où le médicament doit agir. Certains excipients sont dotés d'effets notoires, qui peuvent être à l'origine de manifestations allergiques, ou d'intolérance d'où parfois, les différences de tolérance entre les médicaments génériques et les médicaments princeps (dans les 2 sens : un médicament princeps peut être mieux toléré ou, inversement, moins bien toléré qu’un médicament générique).
Les vaccins
Un vaccin est une préparation administrée pour provoquer l’immunité contre une maladie en stimulant la production d’anticorps. On trouve dans les vaccins des suspensions de micro-organismes inactivés ou atténués, ou des produits ou dérivés de micro-organismes. L’injection est la voie d’administration la plus courante, mais certains vaccins sont donnés par voie orale ou en pulvérisations nasales (définition de l'OMS).
Conseils pratiques
- Un vaccin doit être conservé à une température comprise entre 2°C et 8°C, c’est-à-dire dans un réfrigérateur ;
- un vaccin qui a congelé (stocké à 0°C) parce qu'il a été placé trop près du compartiment à glace est INEFFICACE. Assurez-vous que le réfrigérateur n'est pas trop froid !
- Si vous emmenez votre vaccin chez le médecin dans une glacière, assurez-vous que la boîte contenant le vaccin n'est pas en contact direct avec la glace (trop froid pour le vaccin) ;
- le vaccin résiste mieux à une température trop élevée que trop basse, il peut donc rester à température ambiante durant votre passage dans la salle d'attente du médecin.
Pour en savoir plus sur les vaccins des voyageurs, contactez le Centre Santé et Voyages.
Les contraceptifs
Il existe de très nombreux contraceptifs : préservatifs, hormones ou dispositifs intra-utérins. Les préservatifs sont en vente libre. Les contraceptifs hormonaux ou dispositifs intra-utérins ne peuvent être obtenus que sur ordonnance médicale. Votre médecin généraliste ou gynécologue pourra vous aider à faire le choix adapté à votre cas.
Contraception d’urgence
La contraception d'urgence désigne les méthodes contraceptives qu'une femme peut utiliser pour prévenir la survenue d'une grossesse non prévue après un rapport sexuel non ou mal protégé (échec ou usage défectueux d'une méthode contraceptive comme l'oubli de pilule ou la déchirure d'un préservatif)
Les effets indésirables (EI)
Définitions
Effet indésirable : évènement nocif et non voulu que l’on suspecte d’avoir une relation de causalité avec un médicament (c’est-à-dire que l’on pense et qu’il existe une possibilité raisonnable que l’évènement soit dû au médicament).
Effet indésirable grave : effet indésirable fatal ou susceptible de mettre la vie en danger, ou entraînant une invalidité ou une incapacité importante ou durable, ou provoquant ou prolongeant une hospitalisation, ou se manifestant par une anomalie/malformation congénitale.
Effet indésirable inattendu : effet indésirable dont la nature, la sévérité ou l’évolution ne correspondent pas à ce qui est connu du profil de sécurité du produit (en d’autres termes, qui ne correspondent pas aux informations contenues dans le résumé des caractéristiques du produit).
Pharmacovigilance : surveillance des médicaments et la prévention du risque d’effet indésirable résultant de l’utilisation des médicaments et produits assimilés. La pharmacovigilance comporte :
- le signalement des effets indésirables et le recueil des informations les concernant ;
- l’enregistrement, l’évaluation et l’exploitation de ces informations dans un but de prévention ; ces informations sont analysées en prenant en compte les données disponibles concernant la vente, la délivrance et les pratiques de consommation, de prescription et d’administration aux patients des médicaments et produits ;
- la réalisation de toutes études et de tous travaux concernant la sécurité d’emploi des médicaments.
Pharmacodépendance : dépendance à une ou plusieurs substances actives pouvant aboutir à l’auto-administration de ces substances à des doses produisant des modifications physiques ou comportementales qui constituent des problèmes de santé publique.
Matériovigilance : surveillance des incidents ou des risques d’incidents résultant de l’utilisation des dispositifs médicaux.
Réactovigilance : surveillance des incidents ou des risques d’incidents résultant de l’utilisation des dispositifs médicaux de diagnostic in vitro.
Que faire si on a un EI ?
Si vous pensez avoir un effet indésirable (EI), parlez-en à votre médecin et/ou à votre pharmacien. Ces professionnels de santé vous poseront quelques questions afin de voir s'il est possible que ce soit un EI ou si l'évènement est dû à autre chose. Il est parfois possible, avec des mesures simples, d'éviter l'apparition d'un EI, n'hésitez pas à demander conseil à votre médecin et/ou pharmacien. Lorsqu'il n'y a pas de moyen d'éviter l'EI, le médecin pourra ajuster la dose ou vous proposer une alternative au traitement que vous supportez mal. Le médecin, le pharmacien ou l'infirmière pourra déclarer l'EI à la DASS.
Déclarer un EI, à quoi ça sert ?
La déclaration d’EI permet la collecte de données sur le profil de sécurité d'un médicament afin d'améliorer nos connaissances sur les médicaments et d’évaluer le bénéfice-risque (mettre en balance les bénéfices apportés par rapport aux risques encourus). Ces évaluations permettent, le cas échéant, de mettre en place des mesures pour gérer le risque. Par exemple, si les résultats des analyses montrent que ce sont uniquement les personnes âgées qui souffrent d'un EI particulier, la mesure pourra être d'instaurer une surveillance particulière chez les personnes âgées ou de contrindiquer la prise du médicament par des personnes âgées. Ainsi, le risque est géré dans la population à risque, sans priver les autres patients du médicament. Dans le cas de figure où la prise d'un médicament représente un risque important pour l'ensemble de la population à qui il est destiné et que le bénéfice apporté ne justifie pas cette prise de risque, le médicament est retiré du marché.
Comment déclarer un EI et à qui ?
Les professionnels de santé peuvent (et dans certains cas, doivent) déclarer les EI à la DASS en utilisant le formulaire (formulaire) prévu à cet effet.
Les informations à fournir, dans la mesure du possible, sont :
- Concernant le(la) patient(e) : la date de naissance (ou l’âge), le sexe, les antécédents médicaux (et familiaux lorsque cela est pertinent)
- Concernant le médicament suspecté d’avoir entrainé l’effet : l’indication, la date d’initiation de traitement (à défaut, la durée du traitement jusqu’à la survenue de l’effet), le dosage, le mode d’administration et si le traitement a été maintenu, suspendu temporairement ou définitivement arrêté suite à la survenue de l’effet, ou si il y a eu un ajustement de dosage
- Concernant les traitements pris concomitamment à l’effet mais non suspecté d’en être la cause : l’indication, la date d’initiation de traitement (à défaut, la durée du traitement), le dosage, le mode d’administration, les ajustements de posologie éventuels et, le cas échéant, les arrêts de traitements ayant eu lieu dans le mois précédent la survenue de l’effet,
- Les investigations réalisées (plus il y a de causes possibles éliminées, plus la probabilité que l’effet soit dû au médicament est forte)
- Concernant l’effet : la date de survenue, les circonstances, la description (fournir les résultats d’analyses, les comptes rendus d’hospitalisation etc… lorsque cela est possible), le cas échéant le(s) traitement(s) initié(s) pour traiter l’effet, l’évolution (guérison, guérison avec séquelles, en voie de guérison, non-rétabli, décès, inconnue).
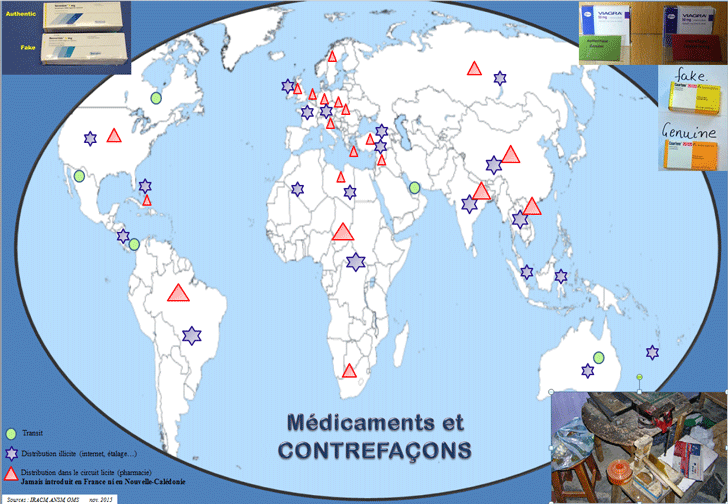
Les contrefaçons de médicaments
Définition
Médicament contrefait : produit dont la composition et les principes actifs ne répondent pas aux normes scientifiques. Il est par conséquent inefficace et souvent dangereux pour le patient (définition OMS). C'est donc :
- un produit contenant d'autres principes actifs que ceux du produit authentique,
- ou un produit contenant des impuretés ou des substances toxiques ;
- ou un produit contenant le ou les bons principes actifs mais au mauvais dosage ;
- un produit dans lequel on ne trouve aucun principe actif;
Risques
La réglementation stricte du circuit du médicament en Nouvelle-Calédonie donne des garanties de sécurité aux usagers. L’achat d’un médicament, d'un complément alimentaire ou de tout « remède » en dehors de ce circuit, notamment sur Internet, expose à des dangers potentiels, possiblement graves, et prive l’usager des conseils adaptés qui peuvent être donnés par les pharmaciens, professionnels du médicament.
La falsification des médicaments comporte des risques d’atteinte à la sécurité et à la santé des patients, la perte de chance d’être soigné par l’absence d’efficacité, le risque d’atteinte à l’hygiène, à l’environnement et à l’éthique. Cela favorise en outre une économie parallèle.
Ampleur
1 médicament sur 10 vendus dans le monde est une contrefaçon ; ce chiffre peut atteindre 7 sur 10 dans certains pays (www.leem.org décembre 2011).
En 2013, les médicaments étaient en tête des produits contrefaits retenus par les douanes européennes (24 % du total), détrônant la contrefaçon de cigarettes.
Les profits engendrés par la contrefaçon de médicaments s'élevaient à 75 milliards de dollars en 2010, soit un montant supérieur à ceux issus du trafic de stupéfiants.
Conseils aux voyageurs
Avant le séjour :
- préparez une trousse de voyage adaptée à votre destination ;
- en cas de maladie chronique, emportez votre traitement en quantité supérieure à celle nécessaire pour la durée du séjour ;
- demandez à votre médecin des ordonnances en dénomination commune internationale (DCI) et gardez-les accessibles dans votre bagage à main, avec les médicaments indispensables ;
- répartissez les autres médicaments dans vos bagages, gardez les emballages.
Pendant le séjour :
- en cas de problème de santé, consultez un médecin (listes disponibles dans les ambassades) ;
- tout achat de médicament ne doit s’effectuer que dans les circuits officiels de distribution ;
- assurez-vous de l’intégrité de l’emballage et de l’absence d’anomalie visible sur la boîte, la notice, le blister… Signalez toute anomalie au pharmacien ;
- un prix très bas peut être le signe d’un faux médicament (mais certains faux coûtent cher)!
- en cas d’effet indésirable, consultez un médecin ;
- n’achetez que les quantités nécessaires.
Le guide des anti-infectieux
Ce guide d’utilisation des anti-infectieux en Nouvelle Calédonie a été élaboré en fonction des spécificités de résistance bactérienne du territoire.
Sauf précision, ce guide est applicable hors grossesse et hors pédiatrie.
Les propositions thérapeutiques de ce guide ciblent prioritairement l’antibiothérapie probabiliste initiale qui devra être impérativement réévaluée à 48h en fonction :
• De l’évolution clinico-biologique du patient et la tolérance du sepsis et des thérapeutiques ;
• Des résultats microbiologiques ;
• Des résultats para-cliniques.